Resumo
A hemorragia grave com necessidade de transfusão de sangue e componentes é uma complicação frequente na unidade de terapia intensiva e está associada ao aumento da morbidade e da mortalidade. A identificação adequada e o tratamento precoce da causa específica da coagulopatia tornam-se fundamentais para o controle efetivo da hemorragia, racionalizando a utilização de sangue e componentes, e desta forma, prevenindo a ocorrência de efeitos adversos. Testes convencionais da coagulação (tempo de ativação de protrombina e tempo de tromboplastina parcial ativada) apresentam limitações para prever sangramento e guiar a terapia transfusional em pacientes graves. Testes viscoelásticos como a tromboelastografia e tromboelastometria rotacional permitem a rápida detecção da coagulopatia e orientam a terapia de forma individualizada, alvo dirigida com drogas hemostáticas específicas. A nova era da tromboelastometria confia na sua eficácia, praticidade, reprodutibilidade e custo-eficácia para se firmar como a principal ferramenta diagnóstica e guia transfusional em pacientes com sangramento ativo grave.
Introdução
Inúmeras doenças encontradas na unidade de terapia intensiva ou no centro cirúrgico podem comprometer o sistema de coagulação. Hemorragia grave com necessidade de transfusão de sangue e componentes é uma manifestação clínica frequente, muitas vezes levando a um desfecho clínico indesejável (1). Tradicionalmente, a prática de transfusão de sangue e componentes tem sido indicada com base em testes convencionais de coagulação em associação com sinais clínicos de sangramento ativo (2,3). Coagulopatia, definida como redução na contagem de plaquetas, nos tempos de coagulação e na concentração de fibrinogénio, é comum em doentes graves, aumentando o risco de transfusão de sangue e componentes. Transfusão de plasma fresco congelado está associada a um aumento em três vezes o risco de infecção nosocomial em pacientes cirúrgicos graves (4). Transfusão de concentrado de plaquetas, glóbulos vermelhos e/ou plasma fresco congelado está associada a um maior risco de insuficiência pulmonar aguda (5).
O sistema hemostático é composto pelo endotélio, proteínas solúveis do sangue, plaquetas, sistema fibrinolítico e anti-fibrinolítico, responsáveis pela ativação, modulação e lise do coágulo. O modelo celular de coagulação, descrito em 2001 por Hoffman et al., demonstra que o complexo processo de formação de coágulo é desencadeado pelo fator tecidual e envolve quatro fases consecutivas: iniciação, amplificação, propagação e estabilização do coágulo (6).
O sistema de coagulação, no cenário de pacientes graves tem sido tradicionalmente avaliado através dos testes convencionais da coagulação como o tempo de protrombina, índice normalizado internacional (INR), tempo de trombina e o tempo de tromboplastina parcial ativada (3). Embora os testes convencionais da coagulação não tenham sido validados para prever e/ou orientar a terapia na hemorragia aguda (adquirida), mas foram validados para monitorar a terapia com antagonistas de vitamina K e heparina; os testes convencionais da coagulação têm sido amplamente utilizados para este fim (7).
A ausência de trombomodulina, expressa pelas células endoteliais, responsável pela ativação da via da proteína C, inibidor natural da coagulação, limita a avaliação dos testes convencionais da coagulação. Desta forma, estes testes avaliam apenas a geração de trombina determinada pelos fatores pró-coagulantes, sendo incapazes de demonstrar o equilíbrio hemostático entre fatores ativadores e inibidores da coagulação (8,9).
Testes convencionais de coagulação são realizados em amostra de plasma, não levam em consideração a interação dos fatores da coagulação com as plaquetas, os elementos celulares do sangue e o endotélio vascular (7). Testes convencionais da coagulação refletem pobre e tardiamente a hemostasia in vivo, pois se alteram quando os fatores de coagulação apresentam déficit maior que 50%. A influência da hipotermia não é mensurada, pois estes testes são realizados a 37°C. Deste modo, distúrbios hemostáticos complexos e multifatoriais, como vistos na hemorragia por trauma, pós-parto, hepatopatias, pós-operatórios e dengue, são difíceis de serem analisados com os testes convencionais da coagulação. Por outro lado, testes viscoelásticos do sangue tornaram-se fundamentais para diagnóstico e manejo terapêutico de pacientes com doença hemorrágica grave. A tromboelastometria rotacional (ROTEM®) aborda estas lacunas fornecendo resultados rápidos, demonstrando a dinâmica da formação, estabilização e dissolução do coágulo, refletindo a hemostasia in vivo à beira do leito (10,11).
A tromboelastografia (TEG®) descrita por Hartert em 1948 na Alemanha, é um método laboratorial que demonstra as alterações viscoelásticas do sangue por meio de uma representação gráfica durante o processo global de formação do coágulo, desde a fase de iniciação, formação, estabilização até sua lise (12). A tromboelastografia (TEG®; Haemoscope Corporation, IL, EUA) e/ou a tromboelastometria rotacional (ROTEM®, TEM International GmbH, Munich, Germany) utilizam sangue total, demonstrando as interações entre as diferentes células do sangue, suas características bioquímicas e podem ser realizada na temperatura do paciente (2).
As primeiras descrições de aplicabilidade do TEG® foram no transplante hepático (13). Mais tarde, foram descritas em cirurgia cardíaca (14). Em pacientes com trauma, a tromboelastografia demonstrou prever necessidades de transfusão (15). Nos anos 1990, surge a tromboelastometria rotacional, um aperfeiçoamento da tromboelastografia, um sistema mais resistente às vibrações, permitindo seu deslocamento a beira do leito. O sistema ROTEM® possui um computador integrado para análise automatizada, uma pipeta eletrônica e quatro canais para aferições simultâneas. O emprego de novos reagentes, inibidores e ativadores, acelerou o resultado do exame e permitiu a identificação de diferentes distúrbios da coagulação. Desta forma, a tromboelastometria passou a guiar a terapia hemostática através de metas, de acordo com a necessidade de cada paciente (2).
Hemorragia maciça e transfusão de sangue estão associadas ao aumento da morbidade, da mortalidade e dos custos (16,19). Testes viscoelásticos do sangue (TEG® e ROTEM®) podem racionalizar hemotransfusões e otimizar o tratamento de pacientes graves com sangramento ativo, por guiar e individualizar a terapêutica, justificando o investimento desta tecnologia custo efetiva (20,21). A nova era da tromboelastometria confia na sua praticidade, reprodutibilidade e custo-efetividade para se firmar como a principal ferramenta diagnóstica e guia transfusional em pacientes com sangramento ativo grave.
Metodologia dos testes viscoelásticos
Para a realização de testes viscoelásticos (ROTEM® ou TEG®), é necessária uma amostra de sangue total citratado coletado por punção venosa de sangue periférico. Podem ser realizados na temperatura do paciente, o que representa uma vantagem em pacientes com discrasia sanguínea relacionada à hipotermia.
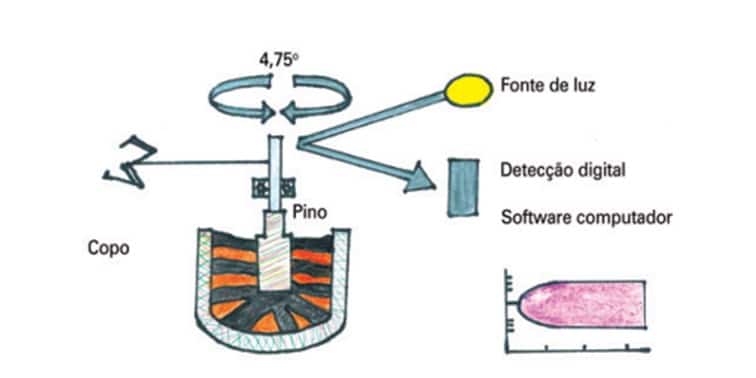
O princípio da tromboelastografia envolve a incubação de 360uL de sangue total a 37°C, em um copo cilíndrico aquecido. O copo oscila durante 10 segundos em um ângulo de 4°45’ com um pino suspenso livremente em um copo por um fio de torção (Figura 1).
Figura 1. Representação esquemática da análise pela tromboelastometria rotacional.
Ocorrem, então, alterações bioquímicas de pH, eletrólitos e temperatura, promovendo a interação entre células do sangue e a subsequente ligação entre fibrinas e plaquetas, que, pelo movimento rotativo do copo, transmite uma cadência de movimento para o pino imerso. Deste modo, a magnitude da expressão gráfica está diretamente relacionada com a resistência do coágulo formado. Após a retração do coágulo, ocorre sua lise. As ligações são quebradas, e a transferência do movimento do copo é reduzida. O movimento de rotação do pino através do transdutor mecânico é convertido a um sinal elétrico, graficamente manifesto (Figura 2).
Com o ROTEM®, ao contrário da TEG®, é o pino de aço que faz uma rotação em 4°75’ em relação ao copo. Por meio de uma leitura óptica, esta movimentação transmite para um software uma representação gráfica de amplitude em relação ao tempo de todo o processo de formação do coágulo, desde a iniciação, a máxima formação, até sua lise (Figura 1). A vantagem que o ROTEM® oferece é sua capacidade de apresentar resultados mais rápidos, a partir de 5 a 10 minutos, e identificar o distúrbio específico da coagulação em virtude dos testes reagentes; aceleradores e inibidores do processo de formação do coágulo (10).
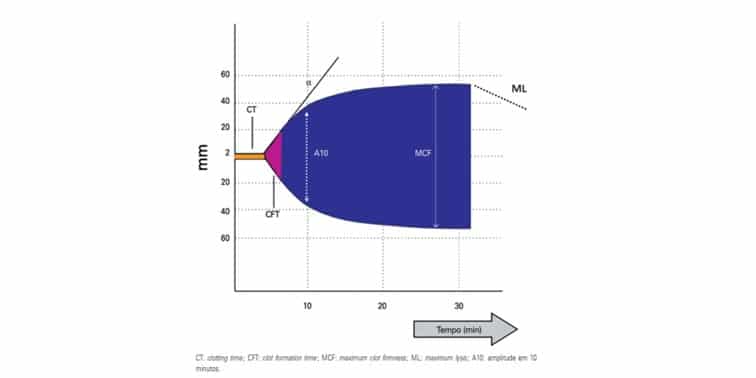
O perfil de coagulabilidade resultante é uma medida de tempo que leva para as primeiras cadeias de fibrina a serem formadas, a cinética de formação do coágulo, a resistência do coágulo e, por fim, sua dissolução. Propriedades físicas do coágulo são dependentes da relação entre fibrinogênio, plaquetas e proteínas do plasma. Este processo produz um traço gráfico característico, que reflete as diferentes fases da coagulação, permitindo sua avaliação qualitativa (Figura 2), (22).
Variáveis e canais para análise Tromboelastometria
A tromboelastometria rotacional é a expressão gráfica do processo de polimerização da fibrina. Desde a formação até a lise do coágulo, suas variáveis são: tempo, dinâmica, tamanho e firmeza do coágulo (Figura 2):
- Clotting time (CT), de zero 0 a 2mm: corresponde ao início da análise do teste até o começo da formação do coágulo. É o início da ativação da tromboplastina, com a formação das primeiras fibrinas, que atingem a amplitude de 2mm. Trata-se da iniciação do coágulo, e da formação inicial de trombina e da polimerização do coágulo. Nesta fase, avaliam-se os fatores de coagulação, assim como o efeito da heparina.
- Clot formation time (CFT), de 2 a 20mm: é o período subsequente ao CT, e representa a cinética da formação de trombina, polimerização da fibrina e estabilização do coágulo por meio do envolvimento das plaquetas, fibrinogênio e fator XIII.
- Ângulo alfa: é a angulação descrita pelo estado de coagulabilidade do paciente. Quanto mais agudo, mais hipocoagulável; quanto mais obtuso, maior a tendência a hipercoagulabilidade.
- Maximum clot firmness (MCF), de 20 a 30mm: período subsequente ao CFT, consiste na amplitude máxima do gráfico. Maior estabilização do coágulo pela polimerização da fibrina. Envolve a interação entre as plaquetas, o fibrinogênio e o fator XIII. Indica a consistência ou a qualidade do coágulo, caracterizando o estado de coagulabilidade do paciente.
- A5 a A30: é a firmeza do coágulo, pela amplitude entre os tempos 5 e 30 minutos.
- Maximum lysis (ML): é a redução da firmeza do coágulo após o MCF. O coágulo é estável se a ML for menor que 15% ou hiper fibrinólise quando maior que 15%.
A aplicabilidade das variáveis descritas se faz nos cinco testes reagentes disponíveis para análise em tempo real da coagulação pelo ROTEM®: INTEM, EXTEM, FIBTEM, HEPTEM, APTEM (Figuras 2 e 3).
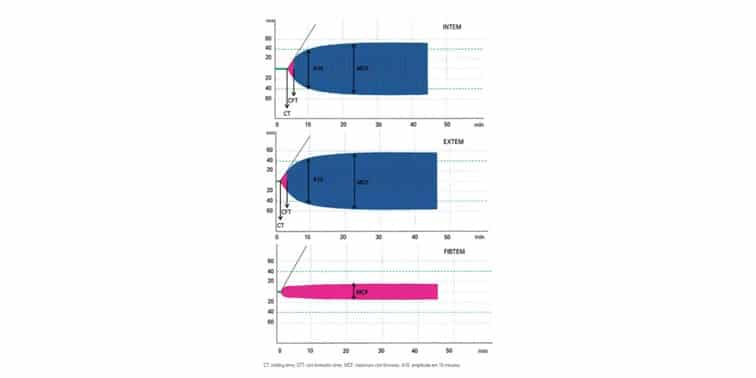
- INTEM: a ativação ocorre na fase de contato pelo ácido elágico. É sensível aos fatores da via intrínseca. Avalia os fatores XII, XI, IX, VIII, X, V, II, I, e von Willebrand. O CT é mais sensível à heparina não fracionada (concentração >0,15U/mL no sangue).
- XTEM: ativação pela tromboplastina ou fator tissular (cérebro de coelho). Início da formação do coágulo em 70 segundos. É mais sensível à fibrinólise. Teste de triagem de via extrínseca: tempo de protrombina (fatores vitamina K-dependentes: II, VII, IX, X). O CT é menos sensível à heparina (concentração >4U/mL de heparina não fracionada no sangue).
- FIBTEM: ativação similar ao EXTEM. A adição de citocalasina D inibe a função plaquetária, permitindo a avaliação isolada do fibrinogênio. O coágulo resultante é dependente apenas da formação e da polimerização da fibrina.
- HEPTEM: ativação semelhante ao INTEM. A adição de heparinase degrada a heparina presente na amostra. Quando o teste de HEPTEM corrige alteração do CT vista no INTEM, define-se como sangue heparinizado, caso contrário, configura-se deficiência de fatores de coagulação.
- APTEM: ativação conforme EXTEM. Pela adição de aprotinina ao reagente, ocorre inibição da fibrinólise. Caso haja correção do ML em relação ao EXTEM, caracteriza-se a hiper fibrinólise verdadeira (ML>15%) (2,23).
Importância da Tromboelastometria
A tromboelastometria avalia de forma global e dinâmica o processo de formação do coágulo, incluindo desde a cinética inicial de geração de trombina, a máxima estruturação e polimerização de fibrina até a lise do coágulo (24,25). Os testes viscoelásticos do sangue detectam precocemente o distúrbio global e específico da coagulação, servindo como guia para a terapia hemostática através de metas com componentes do sangue e/ou agentes hemostáticos (Quadro 1).

Testes convencionais da coagulação, como tempo de protrombina e tromboplastina parcial ativada, são realizados em amostra de plasma, sendo inadequadas para monitorar a coagulopatia, prever sangramento ou guiar a terapia no paciente grave com sangramento ativo. A avaliação em tempo real e funcional da coagulação, com a visualização gráfica de hiper fibrinólise, deficiência de fatores de coagulação, disfibrinogenemia, disfunção plaquetária e efeito de heparina, tornou-se uma realidade na unidade de terapia intensiva (2,23).
Aplicação clínica
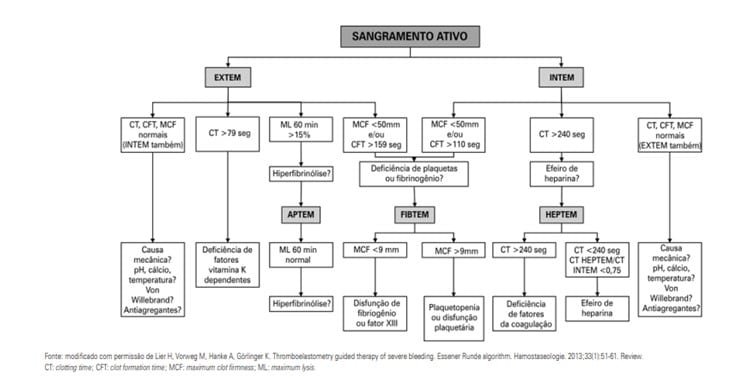
Os exames de screening do ROTEM® são o INTEM e EXTEM. Conforme resultados preliminares, devemos prosseguir a investigação com APTEM e/ou FIBTEM e/ou HEPTEM, conforme proposto por Lier et al., (Figura 4) (2).
Para pacientes apresentando sinais clínicos de sangramento ativo, com parâmetros da tromboelastometria inicialmente normal, deve-se afastar causa mecânica, hipotermia, acidose, hipocalcemia, deficiência de von Willebrand e uso prévio de antiagregantes plaquetários. A não reversão destas etiologias implica coagulopatia de consumo e alterações sequenciais nos perfis tromboelastométricos. No quadro 2, estão suas indicações clínicas.

Os benefícios da terapêutica guiada por metas estendem-se à maior racionalização de hemocomponentes e à redução de seus possíveis efeitos adversos como transfusion-related lung injury (TRALI),(26) transfusionassociated cardiac overload,(27) transfusion-associated immunomodulation, (27) tromboembolismo venoso (TEV), infecções virais e bacterianas (28,29).
Estudo multicêntrico com 1.175 pacientes com trauma contuso e choque hemorrágico subsequente mostrou que plasma fresco congelado (PFC) foi associado de forma independente a aumento de 2,1% e 2,5% na incidência de falência de múltiplos órgãos e da síndrome do desconforto respiratório agudo (SDRA), respectivamente, para cada unidade transfundida (30). A transfusão de PFC está associada à aumento do risco de infecção em pacientes cirúrgicos criticamente enfermos (4).
Estudos demonstram a custo efetividade da utilização do ROTEM® devido a uma redução ou racionalização na utilização dos hemocomponentes, minimizando a ocorrência de efeitos deletérios com as hemotransfusões, com impacto nos custos com o tratamento, no tempo de internação e na mortalidade intra-hospitalar (20).
A tromboelastografia tem limitações de método que devem ser consideradas. A reação ocorre dentro da cuveta, e não no endotélio, em um mecanismo estático de coagulação. Não é sensível ao efeito de antiagregantes plaquetários, anticoagulantes orais, heparina de baixo peso molecular e à deficiência do fator de Von Willebrand (23).
Conclusão
A nova era da tromboelastometria é agora, trazendo uma significativa mudança no paradigma da análise do sistema de coagulação à beira leito. Terapia hemostática precoce guiada por metas é uma necessidade para os pacientes graves com coagulopatia. Sugerimos a utilização de rotina da tromboelastometria rotacional, confiando na sua reprodutibilidade, custo-efetividade e segurança, como ferramenta diagnóstica dos distúrbios da coagulação, orientando o manejo terapêutico individualizado em pacientes graves com sangramento ativo.
Referências
1. Lee TH, Hampton DA, Diggs BS, McCully SP, Kutcher M, Redick BJ, et al. Traumatic brain injury is not associated with coagulopathy out of proportion to injury in other body regions. J Trauma Acute Care Surg. 2014;77(1):67-72; discussion 72.
2. Lier H, Vorweg M, Hanke A, Görlinger K. Thromboelastometry guided therapy of severe bleeding. Essener Runde algorithm. Hamostaseologie. 2013;33(1): 51-61. Review.
3. Levi M, Schultz M. Coagulopathy and platelet disorders in critically ill patients. Minerva Anestesiol. 2010;76(10):851-9. Review.
4. Sarani B, Dunkman WJ, Dean L, Sonnad S, Rohrbach JI, Gracias VH. Transfusion of fresh frozen plasma in critically ill surgical patients is associated with an increased risk of infection. Crit Care Med. 2008;36(4):1114-8.
5. Khan H, Belsher J, Yilmaz M, Afessa B, Winters JL, Moore SB, et al. Fresh frozen plasma and platelet transfusions are associated with development of acute lung injury in critically ill medical patients. Chest. 2007;131(5):1308-14.
6. Hoffman M, Monroe DM 3rd. A cell-based model of hemostasis. Thromb Haemost. 2001;85(6):958-65.
7. Levi M, Schultz M, van der Poll T. Coagulation biomarkers in critically ill patients. Crit Care Clin. 2011;27(2):281-97.
8. Tripodi A, Primignani M, Chantarangkul V, Dell’Era A, Clerici M, de Franchis R, et al. An imbalance of pro- vs anti-coagulation factors in plasma from patients with cirrhosis. Gastroenterology. 2009;137(6):2105-11.
9. Tripodi A, Salerno F, Chantarangkul V, Clerici M, Cazzaniga M, Primignani M, et al. Evidence of normal thrombin generation in cirrhosis despite abnormal conventional coagulation tests. Hepatology. 2005;41(3):553-8.
10. Song JG, Jeong SM, Jun IG, Lee HM, Hwang GS. Five-minute parameter of thromboelastometry is sufficient to detect thrombocytopenia and hypofibrinogenaemia in patients undergoing liver transplantation. Br J Anaesth. 2014;112(2):290-7.
11. Woolley T, Midwinter M, Spencer P, Watts S, Doran C, Kirkman E. Utility of interim ROTEM(®) values of clot strength, A5 and A10, in predicting final assessment of coagulation status in severely injured battle patients. Injury. 2013;44(5):593-9.
12. Hartert H. [Not Available]. Klin Wochenschr. 1948;26(37-38):577-83. Undetermined Language.
13. Kang YG, Martin DJ, Marquez J, Lewis JH, Bontempo FA, Shaw BW Jr, et al. Intraoperative changes in blood coagulation and thrombelastographic monitoring in liver transplantation. Anesth Analg. 1985;64(9):888-96.
14. Spiess BD, Gillies BS, Chandler W, Verrier E. Changes in transfusion therapy and reexploration rate after institution of a blood management program in cardiac surgical patients. J Cardiothorac Vasc Anesth. 1995;9(2):168-73.
15. Kaufmann CR, Dwyer KM, Crews JD, Dols SJ, Trask AL. Usefulness of thrombelastography in assessment of trauma patient coagulation. J Trauma. 1997;42(4):716-20; discussion 720-2.
16. Murphy GJ, Reeves BC, Rogers CA, Rizvi SI, Culliford L, Angelini GD. Increased mortality, postoperative morbidity, and cost after red blood cell transfusion in patients having cardiac surgery. Circulation. 2007;116(22):2544-52.
17. Aronson D, Dann EJ, Bonstein L, Blich M, Kapeliovich M, Beyar R, et al. Impact of red blood cell transfusion on clinical outcomes in patients with acute myocardial infarction. Am J Cardiol. 2008;102(2):115-9.
18. Marik PE, Corwin HL. Efficacy of red blood cell transfusion in the critically ill: a systematic review of the literature. Crit Care Med. 2008;36(9):2667-74. Review. Erratum in: Crit Care Med. 2008;36(11):3134.
19. Christensen MC, Krapf S, Kempel A, von Heymann C. Costs of excessive postoperative hemorrhage in cardiac surgery. J Thorac Cardiovasc Surg. 2009;138(3):687-93.
20. Spalding GJ, Hartrumpf M, Sierig T, Oesberg N, Kirschke CG, Albes JM. Cost reduction of perioperative coagulation management in cardiac surgery: value of “bedside” thrombelastography (ROTEM). Eur J Cardiothorac Surg. 2007;31(6):1052-7.
21. Görlinger K, Fries D, Dirkmann D, Weber CF, Hanke AA, Schöchl H. Reduction of Fresh Frozen Plasma Requirements by Perioperative Point-of-Care Coagulation Management with Early Calculated Goal-Directed Therapy. Transfus Med Hemother. 2012;39(2):104-13.
22. Mallett SV, Cox DJ. Thrombelastography. Br J Anaesth. 1992;69(3):307-13. Review.
23. Lang T, von Depka M. [Possibilities and limitations of thrombelastometry/- graphy]. Hamostaseologie. 2006;26(3 Suppl 1):S20-9. German.
24. Luddington RJ. Thrombelastography/thromboelastometry. Clin Lab Haematol. 2005;27(2):81-90. Review.
25. Salooja N, Perry DJ. Thrombelastography. Blood Coagul Fibrinolysis. 2001; 12(5):327-37. Review. Erratum in: Blood Coagul Fibrinolysis. 2002;13(1):75.
26. Murphy EL, Kwaan N, Looney MR, Gajic O, Hubmayr RD, Gropper MA, et al. Risk factors and outcomes in transfusion-associated circulatory overload. Am J Med. 2013;126(4):357.e29-38.
27. Görlinger K, Saner FH. Prophylactic plasma and platelet transfusion in the critically Ill patient: just useless and expensive or even harmful? BMC Anesthesiol. 2015;15:86. Review.
28. Nienaber U, Innerhofer P, Westermann I, Schöchl H, Attal R, Breitkopf R, et al. The impact of fresh frozen plasma vs coagulation factor concentrates on morbidity and mortality in trauma-associated haemorrhage and massive transfusion. Injury. 2011;42(7):697-701.
29. Schöchl H, Nienaber U, Maegele M, Hochleitner G, Primavesi F, Steitz B, et al. Transfusion in trauma: thromboelastometry-guided coagulation factor concentrate-based therapy versus standard fresh frozen plasma-based therapy. Crit Care. 2011;15(2):R83.
30. Watson GA, Sperry JL, Rosengart MR, Minei JP, Harbrecht BG, Moore EE, Cuschieri J, Maier RV, Billiar TR, Peitzman AB; Inflammation and Host Response to Injury Investigators. Fresh frozen plasma is independently associated with a higher risk of multiple organ failure and acute respiratory distress syndrome. J Trauma. 2009;67(2):221-7; discussion 228-30.
Artigo original publicado pelo Journal Einsten no ano de 2017, pelos autores Tomaz Crochemore, Felipe Maia de Toledo Piza, Roseny dos Reis Rodrigues, João Carlos de Campos Guerra, Leonardo José Rolim Ferraz, Thiago Domingos Corrêa. Conheça o nosso blog para ler mais conteúdos!